LENK-VPX
Nuklidkarte - Poster, Vollversion, englisch
Die Vollversion der blume Nuklidkarte stellt über 3.000 experimentell nachgewiesene Nuklide mit mehr als 10.000 präzisen Datensätzen dar, basierend auf den Daten des National Nuclear Data Center (Brookhaven, USA).
Die klare, wissenschaftlich fundierte Darstellung mit quadratischer Kachelung, optimierter Farbgebung sowie farblich gekennzeichneten Zerfallsarten ermöglicht eine umfassende Übersicht für Studium, Lehre und Forschung. Geeignet für Hochschulen, Forschungseinrichtungen und anspruchsvollen Unterricht.
Ausführung
- • Hochwertiger Druck auf Qualitätspapier
• UV-Lack-Veredelung (kratz- und UV-beständig)
• Strukturierte Achsendarstellung (Ordnungszahl / Neutronenzahl)
Gewicht: 400 g
Material: hochwärtige Papierqualität
Weitere Versionen erhältlich: Schülerversion englisch, Schülerversion, Vollversion
Für jedes Nuklid sind, soweit bekannt, folgende Werte angegeben:
- • Elementsymbol
• Massenzahl A
• Ordnungszahl Z
• Neutronenzahl N
• Halbwertszeit
• Energie der Zerfallsart
• Anteil am natürlichen Vorkommen (stabile Nuklide)
• relative Häufigkeit der Zerfallsart durch farbliche Unterteilung
• Metastabile Zustände
• Absorptions-/ Spaltungsquerschnitte
- • α
• β-
• β+/ Elektroneneinfang
• γ (Isomerer Übergang)
• Spontanspaltung
• Protonenemission
• Neutronenemission
• Clusteremission
Produktart
Poster
Ausführung
Vollversion
Sprache
Englisch
Pack à 1 Stück
Preis pro Pack (Incl. MwSt.):
ab
CHF 113.51
Produktempfehlungen
LMEK-PA2
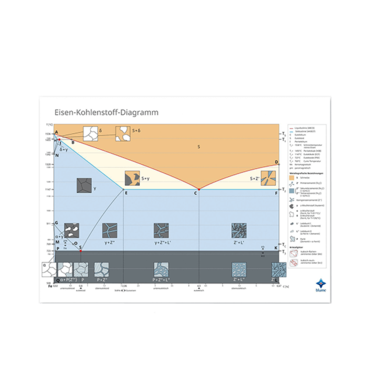
Eisen-Kohlenstoff-Diagramm - Poster DIN A2
Das Eisen-Kohlenstoff-Diagramm (Fe–Fe₃C) veranschaulicht die Eigenschaften und das Verhalten von Eisenwerkstoffen wie Stahl und Gusseisen in Abhängigkeit vom Kohlenstoffgehalt. Als Gleichgewichtsschaubild des metastabilen Systems bietet es eine klare Darstellung von Phasenfeldern, Gefügezusammensetzungen, Temperaturbereichen und relevanten Umwandlungspunkten bis 6,67 % Kohlenstoff. Farblich differenzierte Bereiche, strukturierte Gefügebilder sowie ergänzende Details zu Magnetismus und Kristallgitter erleichtern das Verständnis. Durch hochwertige Druck- und Papierqualität mit UV-Lack-Veredelung ist das Poster besonders widerstandsfähig und ideal für Studium, Lehre und Praxis im werkstofftechnischen Bereich.Inhalt
- • x-Achse: Massenprozent des Kohlenstoffs; y-Achse: Temperatur
• Metastabiles System
• Signifikanten Punkte und Linien sind angegeben sowie die einzelnen Phasenfelder erläutert
• Relevante Temperaturen und Massenprozente werden hervorgehoben und durch Linien gekennzeichnet
• Die wichtigsten Temperaturbereiche sind zusätzlich farblich voneinander getrennt
• Metallografische Bezeichnungen und Zusammensetzungen der Mischkristalle und Gefüge werden übersichtlich dargestellt
• Einzelne Phasen, Struktur und Zusammensetzungen detailliert im Gefügebild durch Farben und Muster optisch nachvollziehbar
• Bezeichnung der Eisenwerkstoffe und Zusammensetzungen nach Kohlenstoffgehalt
• Details wie Magnetismus und Kristallgitter anschaulich dargestellt
Produktgruppe
SL
Produkt
EK
Ausführung
PO
Spezifikation
A2
Deckel / Stopfen
D
ab
CHF 25.94
LMAB-LA4-30
Anorganik Basics, Lerntafel DIN A4, Klassensatz à 30 Stk.
Die Lerntafel Anorganik Basics fasst die zentralen Themen der anorganischen Chemie übersichtlich und klar strukturiert zusammen. Sie unterstützt Studierende im Grundstudium sowie Schülerinnen und Schüler im Abitur bei der gezielten Prüfungsvorbereitung und dient auch darüber hinaus als hilfreiche Gedächtnisstütze.
Die kaltkaschierte PET-Laminierung macht die Tafel besonders strapazierfähig und langlebig, ideal für den regelmässigen Einsatz im Studium und Beruf.
Folgende Themen werden dargestellt:
- • Massenwirkungsgesetz
• Löslichkeitsprodukt
• Ionenprodukt des Wassers
• Säuren und Basen
• pH-Wert
• Pufferlösungen
• Titrationsgleichung/-kurve
• Konzentrationsberechnungen
• Atommodell
• chemische Bindungen
• starke/schwache Bindungen
• Periodensystem (Regeln, die sich aus dem Periodensystem ableiten lassen für: Elektronegativität, Atomradius, Ionisierungsenergie, Elektronenaffinität und Hydratationsradius)
• Strukturformeln
• Orbitalformen
• Elektronenkonfiguration
• VSEPR-Modell (EPA)
• Atomaufbau
• Elektronegativität
• Oxidationszahl
• Redoxreaktion
• Elektrochemische Spannungsreihe
• Nernst‘sche Gleichung
• Radioaktive Strahlung
• Thermodynamik (Satz von Hess, Hauptsätze)
• Gasgesetz
Produktgruppe
SL
Produkt
AB
Ausführung
PO
Spezifikation
A4
Deckel / Stopfen
D
ab
CHF 168.64
CuL-Kit-Student
Kit Student
Einsteigerfreundliches Set für Schülerinnen und Schüler, ideal für Einzel- oder Partnerarbeit. Vermittelt chemische Grundlagen durch praktische Experimente rund um Licht und Reaktionen und eignet sich für Unterricht, Projekte und Workshops.Produktgruppe
SL
Produkt
CK
ab
CHF 518.88